GC 녹십자는 1 분기 내 데이터 정리를 마친 후 4 월에 허가 신청을 할 계획이다.
(서울 = 연합 뉴스) 김 잔디 기자 = 종근당[185750]신종 코로나 바이러스 감염증 (코로나 19) 치료제 ‘나 파벨 탄주'(성분명 나파 모 스타트 메실 레이트)가 조건부 면허로 술을 마신 ‘국내 2 호’치료를 누가 대신 할 것인가에 대해 많은 관심을 받고있다.
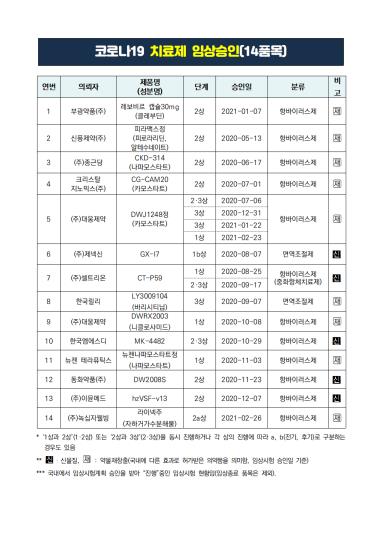
18 일 식품 의약품 안전 처에 따르면 국내에서 승인 된 코로나 19 치료제는 길르앗 사이언스 코리아의 베큘 리주 (성분명 렘 데시 비르)와 셀트리온의 레 키로 나주 (성분명 regdanvimab) 두 종류가있다.
이 중 지난달 5 일 승인 된 레 키로 나주는 국내에서 개발 된 ‘국내 1 호’코로나 19 치료제 다.
종근당, GC 녹십자, 대웅 제약은 셀트리온이 처음으로 영예를 얻은 이래 국내 제 2 제약의 자리를 차지한 국내 제약사로 꼽힌다.
이후 종근당은 이달 8 일 식품 의약품 안전 처에 품목 허가를 신청 해 가장 앞선다는 평가가 많았다.
종근당의 승인에 실패했지만 국내 COVID-19 치료제에 대한 기대감은 감소했지만 GC 녹십자는 코로나 19 혈액 시스템 약물 허가 최종 신청을 진행 중이다.
지씨 녹십자는 지난해 12 월 31 일 임상 2 상 피험자를 대상으로 코로나 19 혈액 계통 신약 ‘GC5131A’의 약물 투여를 완료했으며 지금까지 관련 자료를 분석 요약했다.
GC 녹십자 관계자는 “현재 자료 정리 중”이라며 “1 분기 내 분석을 마친 후 4 월 식품 의약품 안전 처에 허가를 신청할 계획”이라고 말했다.
GC 녹십자의 코로나 19 혈액 치료 시스템이 식약 처의 치료 용 승인을 통해 의료 분야 환자들이 사용하고 있다는 사실은 승인 전 기대감을 높이고있다. 지난해 10 월부터 올해 3 월 9 일까지 총 41 건의 치료 목적이 승인됐다.
식품 의약품 안전 처는 중증, 생명을 위협하는 환자의 치료 또는 기타 치료 수단에 대한 허가를받지 않은 임상 시험용 의약품을 사용자가 사용할 수 있도록 치료 목적 사용 승인 시스템을 운영하고 있습니다.
대웅 제약도 코로나 19 치료제로 Hoystar 정제 (성분명 chamostatmesylate)를 개발하기 위해 2/3 상 임상 시험을 진행 중이다.
특정 허가 신청 계획은 공개되지 않았습니다. 대웅 제약도 Hoystar 정제가 코로나 19 예방에 미치는 영향을 확인하기 위해 3 상을 병행하고있다.
또한 국내 제약사 중 부광 제약은[003000], 신풍 제약[019170], 크리스탈 유전체학[083790], 동화 약품[000020], 면역, 녹십자 건강[234690] Et al. COVID-19 치료제 개발을위한 임상 2 상을 진행하고 있습니다.
![[식품의약품안전처 제공. 재판매 및 DB 금지]](https://i0.wp.com/img5.yna.co.kr/etc/inner/KR/2021/03/17/AKR20210317183900017_01_i_P4.jpg?w=600&ssl=1)
[식품의약품안전처 제공. 재판매 및 DB 금지]
무단 전재, 재배포 금지>
2021/03/18 07:00 전송