단백질 독성 스트레스 반응을 조절하는 MARK 2 효소
MARK 2를 자극하는 PKC 델타 효소도 … Journal’PLoS Biology ‘paper

파킨슨 병 및 알츠하이머 병과 같은 신경 퇴행성 환자 또는 노인의 뇌에서 많은 변형 된 양친 매성이 관찰됩니다.
전분 영양 체의 정상적인 구조는 뇌의 폐기물 배출 용기로도 사용됩니다.
[스페인 바르셀로나대 제공/ 재판매 및 DB 금지]
(서울 = 연합 뉴스) 한기천 기자 = 전 세계적으로 알츠하이머 병, ALS (일명 루게릭 병) 등 신경 퇴행성 질환을 앓고있는 사람이 5 천만 명 이상으로 추정된다.
그럼에도 불구하고 신경 퇴행성 질환의 기초 약물 외에 질병의 진행을 늦출 수있는 치료법은 없습니다.
무엇보다 신경 퇴행성 질환의 원인을 정확히 알지 못하기 때문입니다.
존스 홉킨스 대학의 블룸버그 공중 보건 대학 과학자들은 세포의 스트레스 반응을 조절하는 “분자 전환”효소를 발견했습니다.
세포의 스트레스 반응은 세포 사멸 및 신경 퇴행성 질환을 유발하는 강력한 요인으로 간주됩니다.
MARK 2라고 불리는이 효소는 신경 퇴행성 질환 치료제를 찾는 과학자들에게 새로운 표적이 될 가능성이 높습니다.
이번 연구 결과는 11 일 (현지 시간) 동료 심사 저널 ‘PLoS Biology’에 게재됐다.
연구팀은 신경 퇴행성 질환의 핵심 특징 인 단백질 독성 스트레스에 대한 세포 반응에 초점을 맞추 었습니다.

ALS는 UBQLN2 유전자의 돌연변이와 관련이 있습니다.
이 유전자는 잘못 접힌 단백질과 같은 세포 노폐물의 처리를 조절하는 것으로 알려져 있습니다.
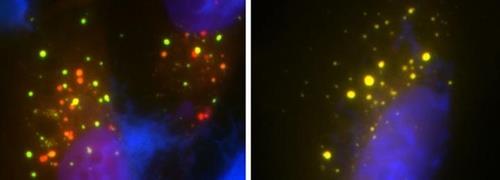
UBQLN2 유전자가 정상인 왼쪽 세포의 빨간색 점은 쓰레기 제거 경로가 잘 작동 함을 나타냅니다.
돌연변이의 오른쪽 셀에는 빨간 점이 보이지 않습니다.
[미 메릴랜드 의대 제공 / 재판매 및 DB 금지]
단백질 독성 스트레스는 세포의 주요 영역에서 손상된 (잘못 접힌) 단백질의 축적입니다.
세포가 단백질 독성 스트레스에 적극적으로 반응하면 생산되는 단백질의 양이 감소하고 스트레스를 극복 할 수 있습니다.
그러나 스트레스 반응에 문제가 발생하여 단백질 합성의 감소가 장기간 지속되면 세포가 단백질 결핍에 빠지게되어 세포가 손상되고 세포가 죽게됩니다.
반대로 너무 많은 단백질은 단백질 독성 스트레스 반응 없이도 세포 손상과 사망을 유발할 수 있습니다.
따라서 연구팀은 단백질 독성 스트레스를 감지하여 스트레스 반응 스위치를 조작하는 신호 경로를 확인하는 것을 목표로했습니다.
우리는 이미이 신호 경로에서 단백질 합성 스위치를 낮추는 몇 가지 키나제가 있다는 것을 알고있었습니다.
그러나 이러한 키나제는 바이러스 감염과 같은 다른 유형의 세포 스트레스 반응에 관여합니다.
연구팀은 이전 연구 결과를 축적 한 데이터베이스를 검색하고 5 개의 후보 키나제를 선택했다. 배양 된 세포와 무 세포 실험을 반복 한 후 MARK 2가 유일한 후보로 선정되었습니다.
MARK 2는 나머지 4 개가없는 상태에서 단백질 독성 스트레스에 반응하고 단백질을 생성하는 세포 시스템을 차단했습니다.

뇌의 성상 세포는 노폐물 제거, 식균 작용 및 신경 조직 복구에 관여합니다.
그러나 신경 퇴행성 질환이 발생하면 성상 세포가 뉴런을 죽입니다.
[뉴욕 줄기세포 재단 연구소 제공 / 재판매 및 DB 금지]
연구진은 신호 경로의 상류를 면밀히 모니터링하여 단백질 독성 스트레스가 발생할 때 MARK 2를 자극하고 활성화하는 PKC 델타라고하는 키나아제를 발견했습니다.
PKC 델타는 단백질 스트레스를 감지하는 센서 역할을했습니다.
실제 알츠하이머 환자의 가족 성 ALS와 척수 조직 샘플을 생성하도록 설계된 마우스 모델에서 테스트했을 때이 PKC 델타 -MARK 2 경로는 매우 강력하게 활성화되었습니다.
연구를 주도한 Jiou Wang은 “ALS에서 PKC delta-MARK 2 경로가 높은 수준으로 활성화되어 단백질 생성을 억제하고 장기적인 질병 과정을 유도합니다.”라고 말했습니다. 그 결과 “그는 지적했다.
Wang의 팀은 또한이 경로가 실제로 신경 퇴행성 질환의 치료 표적이 될 수 있는지 확인하기 위해 ALS 이외의 질병에 대한 연구를 진행할 계획입니다.
왕 교수는 “궁극적으로이 경로는 신경 퇴행성 질환뿐만 아니라 암과 같은 다른 질병과도 관련이있을 수 있다고 생각한다”고 말했다.
무단 전재 재배포 금지>
2021/03/12 17:46 전송