식약청, 본격적인 허가 심사 결과는 검증 자문단 회의 후 2 월 1 일 공개
국내에 도입 예정인 아스트라 제네카의 신종 코로나 19 (코로나 19) 백신이 이번 주말 당국의 첫 번째 전문가 협의 절차를 거친다.

30 일 제약 업계에 따르면 식품 의약품 안전 처는 31 일 오후 ‘코로나 19 백신 안전성 및 유효성 검증 자문단'(이하 검증 자문단이라한다)과 관련한 외부 전문가 간담회를 개최했다. AstraZeneca Corona 19 백신 (AZD1222)에 대한 임상 시험 데이터. 열다.
결과는 2 월 1 일에 공개됩니다.
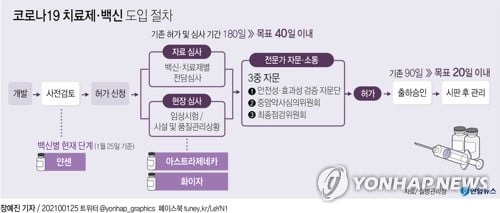
식약 처는 COVID-19 치료제 및 백신에 대한 객관적이고 투명한 승인 검토를 위해 ‘트리플’의 외부 전문가 자문 절차를 마련했습니다.
상담은 검증 자문단, 중앙 약사 심사위원회 (중앙 약사 심사), 최종 심사위원회로 구성된다.
검증 자문회의에서는 감염 의학에 중점을 둔 임상 전문가들이 참여하여 아스트라 제네카 코로나 19 백신의 안전성과 유효성, 임상 적 의의, 대상 환자의 적합성 등을 검토한다.
아스트라 제네카는 올해 1 월 4 일 식약청에 코로나 19 백신 품목 허가를 신청했다.
국내에 도입되는 코로나 19 백신 중 제품 허가를 신청 한 첫 제품이다.
본 제품은 총 2 회 투여되는 백신으로 보관 조건은 2 ~ 8 ℃로 별도의 극저온 시스템을 구축 할 필요없이 기존 시스템으로 배포 할 수 있습니다.
국내 백신 업체 SK 바이오 사이언스와 위탁 생산 계약을 체결 해 수급이 원활 할 것으로 예상된다.
한국은 AstraZeneca와 천만명 백신 구매 계약을 체결했습니다.
그러나 아스트라 제네카 백신의 경우 65 세 이상 노인을 대상으로 한 백신의 효능 논란이 높아져 당국이이 부분을 철저히 검증 할 것으로 알려졌다.
식품 의약품 안전 처는 예방 접종 군과 위약군을 비교 검토하여 65 세 이상 노인의 특별한주의가 필요한 안전 정보가 있는지 확인하고있다.

식품 의약품 안전 처 관계자는 “31 일부터 시작되는 3 중 전문가 협의 절차를 통해 안전성과 유효성을 철저히 검증하겠다”며 “허가 범위에 대한 구체적인 결정은 없다. 아직 전문가 상담이 시작되지 않았습니다. “
29 일 (현지 시간) 유럽 연합 (EU) 집행위원회는 AstraZeneca의 COVID-19 백신의 조건부 판매를 승인했습니다.
화이자와 모데나가 개발 한 백신에 이어 EU에서 조건부 사용을 승인 한 세 번째 COVID-19 백신입니다.
EU의 결정은 EMA (European Medicines Agency)가 18 세 이상의 모든 연령대에 백신에 대한 조건부 판매 승인을 권장 한 지 몇 시간 후에 이루어졌습니다.
EMA는 AstraZeneca 백신이 영국, 브라질 및 남아프리카에서 수행 된 임상 시험 결과를 합친 18 세 이상의 사람들의 COVID-19 예방에 안전하고 효과적인 것으로 밝혀 졌다고 밝혔다.
/ 윤합 뉴스