 |
| 한국 생명 공학 연구원 유권 박사 연구팀은 암으로 인한 섭식 장애의 원인을 규명했다. 사진은 연구팀의 권유 권 박사 (중앙) (명연 제공) © News1 |
한국의 연구원들은 암세포에서 분비되는 특정 단백질이 뇌신경 세포의 특정 수용체를 통해 식욕 조절 호르몬을 조절하는 메커니즘을 발견했습니다.
이는 암 환자의 섭식 장애 원인을 규명하기위한 것으로, 특정 단백질 (Dilp8 / INSL3)에 의해 신호 체계를 조절할 수있는 치료제 개발로 이어질 경우 항암 화학 요법의 효과가 크게 향상 될 것으로 기대됩니다. ).
한국 생명 공학 연구원 (이하 생명 연구소)은 질병 표적 구조 연구 센터 유권 박사 연구팀과 바이오 나노 연구 센터 이규선 박사와 공동 연구를 진행했다. KAIST 서재명 교수 팀과 서울 아산 병원 김성철 (공동 교신 저자)과의 공동 연구. 연구 결과가 나왔다고 18 일 발표했다.
암 환자의 전형적인 합병증 인 암 악액질-식욕 부진 증후군은 심각한 섭식 장애와 지속적인 체중 감소를 동반합니다.
암 환자의 생존과 화학 요법에 악영향을 미치는 것으로 알려져 있지만 암 환자의 섭식 장애의 원인은 밝혀지지 않았습니다.
연구팀은 초파리 암 모델과 RNA 전 사체 분석을 통해 암세포에서 유래 한 특정 단백질 (Dilp8 펩타이드)의 발현과 분비가 크게 증가했음을 확인했다.
또한 뇌신경 세포의 수용체 (Lgr3)를 통한 식욕 조절에 관여하는 신경 펩티드 호르몬의 발현이 변화하여 초파리 암 모델에서 섭식 장애를 유발하는 것으로 나타났다.
이를 바탕으로 KAIST 의과 대학원 서재명 교수 팀은 마우스 암 모델에서도 특정 단백질 (Dilp8 펩타이드)과 상동 인자 인 INSL3이 현저하게 증가하여 섭식 장애를 유발한다는 사실을 발견했다.
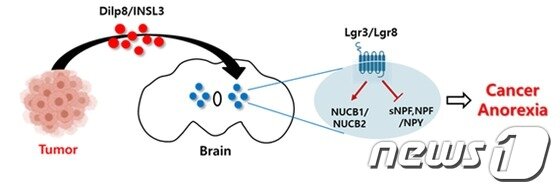 |
| 암으로 인한 섭식 장애 발병 메커니즘 모델 (생명 보험 제공) © News1 |
특히 암세포에서 분비되는 단백질 (INSL3)을 마우스의 뇌에 직접 주입하면 음식물 섭취량과 체중이 감소하는 것을 확인했다.
또한 서울 아산 병원 김송철 교수 팀은 악액질 발생률이 가장 높은 췌장암 환자를 대상으로 임상 관련성 연구를 진행했다.
그 결과 섭식 장애를 보인 췌장암 환자에서 단백질 (INSL3)의 농도가 높은 것을 확인했다.
이 사실은 암세포에서 분비되는 단백질 (INSL3)이 두개 신경계의 식욕 조절에 관여하는 신경 세포에 작용하여 암 환자의 식욕을 감소 시킨다는 것을 알 수있다.
이는 암을 분비하는 물질 인 단백질 (INSL3)이 암 환자의 섭식 장애를 유발하는 중요한 신호 인자로 작용한다는 발견이라고 할 수 있습니다.
유권 연구원은 “암 환자의 전신 쇠약의 현저한 증상 인 악액질 개선에 대한 의학적 수요는 매우 높지만 아직 약물 개발 사례는 없다”고 말했다. 끝났습니다.”
한편,이 연구 스타는 2021 년 2 월 9 일 생물학 분야의 세계적인 학술지 ‘Nature Journal of Cellular Biology’온라인 판에 게재됐다.
